前言本标准按照GB/T 1.1—2009给出的规则编写。本标准代替GB/T 17802—1999《可燃物质动力学常数的热分析试验方法》。 本标准与GB/T 17802—1999相比,主要技术变化如下: ——修改了标准的名称; ——删除了ASTM前言(见1999版的ASTM前言); ——修改了标准的范围(见本版的第1章,1999版的第1章); ——增加了术语和定义(见3.6); ——修改了仪器参数要求中的程序升温速率,由“0.5℃/min~30℃/min”改为“1℃/min~10℃/ min”(见本版的5.1,1999版的6.2); ——增加了试验次数的规定(见7.6)。 本标准中DSC的试验方法和数据处理参考采用了美国ASTM E 698:2001《热不稳定物质阿仑尼 乌斯动力学常数的标准试验方法》(2001年英文版)。 本标准由中华人民共和国公安部提出。 本标准由全国消防标准化技术委员会基础标准分技术委员会(SAC/TC 113/SC 1)归口。 本标准起草单位:公安部天津消防研究所。 本标准主要起草人:陈迎春、邓震宇、卓萍、梁亚东。 本标准所替代标准的历次版本发布情况为: ——GB/T 17802—1999。 1 范围本标准规定了使用差热分析仪(DTA)和差示扫描量热仪(DSC)测量热不稳定性物质放热反应的阿仑尼乌斯方程动力学常数的热分析试验的术语和定义、原理、仪器和材料、试样、试验步骤、数据处理、误差和试验报告。本标准适用于能用阿仑尼乌斯方程和一般速率规律描述的反应。 本标准不适用于曲线偏离直线、部分反应被抑制、同步或连续反应、经历相转变且反应速率在转变温度上十分显著及不能控制的化学反应。 2 规范性引用文件下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T 6425 热分析术语 GB/T 13464—2008 物质热稳定性的热分析试验方法 3 术语和定义GB/T 6425和GB/T 13464—2008界定的以及下列术语和定义适用于本文件。3.1 活化能(E) activation energy 将1 mol 稳定态的分子激发成为1 mol 活化分子所需的能量。 3.2 指前因子(Z) pre-exponential factor 阿仑尼乌斯方程指数前的因子。 3.3 半衰期(t1/2) half-life time 物质能量衰减一半所需要的时间。 3.4 老化 the aged 温度引起物质能量的衰减。 3.5 老化时间 the aged time 试样经历试验过程中每一特定温度下计算的半衰期。 3.6 阿仑尼乌斯方程 Arrhenius equation 反应速率常数和温度之间的数学关系式,表示为: 
4 原理本方法是用差热分析仪或差示扫描量热仪测量物质的焓变温度,计算反应活化能,根据阿仑尼乌斯方程求出反应速率常数,进而求出物质在所需观察温度下的半衰期,并以此来评价物质的热不稳定性。5 仪器和材料5.1 仪器5.2 材料 5.1 仪器差热分析仪(DTA)或差示扫描量热仪(DSC),包含以下主要部件:a) 温度控制器。温度控制器可以控制程序升温速率在1℃/min~10℃/min范围内;温度的控制精度为±2℃,温度的测量精度为±0.5℃。 b) 感应器。感应器应能使温度差或功率差的大小在记录仪上达到40%~95%的满刻度指示。 c) 样品容器。样品容器应不与试样和参比物起反应。一般的样品容器包括铝坩埚、铂坩埚、陶瓷坩埚等。 d) 气体流量控制器。气体流量控制器应能使气体流量控制在10 mL/min~50 mL/min的范围并稳定在5%的误差以内。 e) 冷却装置。冷却装置应能达到-50℃的冷却温度。 f) 压力调节转换器。能够维持试验压力在0.1MPa~1.27MPa范围内,可以测量并调节试验压力至规定值且误差在5%以内。 5.2 材料5.2.1 气源气源包括空气、氮气等,纯度应达到工业用气体纯度。 5.2.2 参比物 参比物在试验温度范围内不发生焓变。典型的参比物有煅烧的氧化铝、玻璃珠、硅油或空容器等。参比物应储存在干燥器中。 6 试样6.1 取样对于液体或浆状试样,混匀后取样即可;对于固体试样,粉碎后用圆锥四分法取样。 6.2 试样量 选择放热量最大值小于8 mJ 的试样量,试样量一般应在0.1 mg~50 mg之间。 7 试验步骤7.1 按GB/T 13464—2008的附录A对仪器的温度测量值进行校准,误差应在±0.5℃范围内。7.2 根据仪器生产者在操作手册中提供的标定程序,标定温度信号精度至±0.5℃,标定热流信号精度至±0.5%。 7.3 将试样和参比物分别放入各自的样品容器中,并使之与样品容器有良好的热接触(对于液体试样,最好加入试样重量20%的惰性材料,如α-氧化铝等)。将装有试样和参比物的样品容器一起放入仪器的加热装置内,并使之与热传感元件紧密接触。 7.4 接通气源,并将气体流量控制在10 mL/min~50 mL/min的范围内(如果在静止状态下进行测量,则不需要通气)。 7.5 根据所用试样的性质和仪器的正常工作温度区间和压力范围来确定试验温度范围和试验压力范围。 7.6 启动升温控制器,在低于试样起始放热温度50℃以下的温度开始对试样以不同的程序升温速率升温,应至少进行四次不同升温速率的试验并记录所有的放热反应峰温Tp。 7.7 对试样进行至少1 h的老化,然后立即冷却到低于老化温度50℃以下。 7.8 对老化后的试样进行7.3~7.6的试验步骤。 8 数据处理8.1 按附录A中给出的方法和示例,对反应峰温进行升温速率(β)、热延迟和非线性校正。8.2 将lgβ与1/T作图(T为校正后的反应峰温)。 8.3 活化能E的近似值按公式(1)计算: 
式中: R——气体常数,8.314 J/(mol·℃)。 8.4 活化能E的精确值计算用数学迭代法按以下步骤进行: a) 近似地计算出E/RT; b) 从表B.2中找出D的对应值; c) 第一次精确的E值按公式(2)计算出: 
d) 重复a)~c)步骤,计算出最后精确的E值。 活化能计算示例参见附录B;活化能计算的替换方法参见附录C;恒温试样计算示例参见附录D。 8.5 阿仑尼乌斯指前因子(Z)按公式(3)计算: 
式中: β——升温速率范围内的中间值。 8.6 不同温度下的速率常数k按公式(4)计算: 
8.7 不同温度下的老化时间t1/2按公式(5)计算: 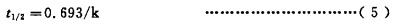
8.8 在相同条件下,如果老化后试样的峰面积是未老化试样峰面积的一半(误差为10%),那么,上述计算出的老化时间就是该物质在该温度下的半衰期。 9 误差最后两次计算出的活化能之间的误差应在±2%内。10 试验报告试验报告应包括下列内容:——试验委托单位名称; ——试验单位名称和试验负责人; ——送样日期和试验日期; ——试样和参比物的名称、组分、重量等; ——仪器型号和样品容器; ——列出升温速率和峰温的关系表; ——反应活化能和半衰期的计算值。 附录A (规范性附录) 峰温的校正方法A.1 峰温校正步骤A.2 峰温校正示例 A.1 峰温校正步骤A.1.1 概述选择一种高纯度金属(通常采用铟),以10℃/min的升温速率升温后得到峰温读数,再把升温速率、热延迟、非线性等三种不同的校正值加到峰温读数中,得到校正后的峰温值。 A.1.2 升温速率校正 通过试验得到各型号仪器不同升温速率的校正值。例如,用一台杜邦990型DTA和一台珀金-埃尔默DSC-2仪器试验得到表A.1所列的校正值。 表A.1 升温速率的校正 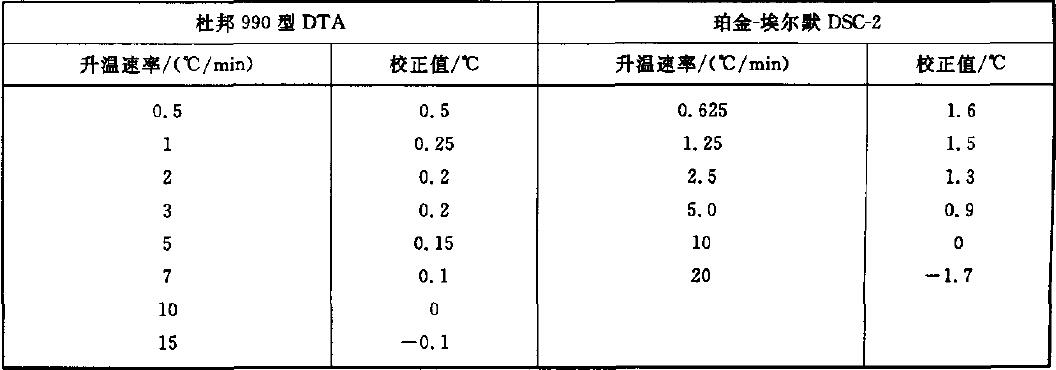
A.1.3 热延迟校正 按照公式(A.1)用仪器灵敏度乘以峰高和热阻,得到热延迟校正值TLe, 
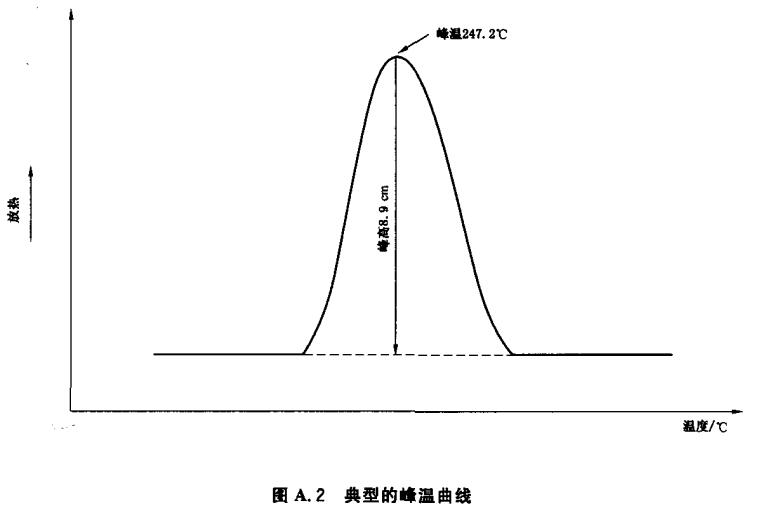
式中: S——灵敏度,mW/cm; H——峰高,cm; R0——热阻,℃/mW。 根据试验(见图A.1),R0值由线段a和线段b比值决定;斜线是由曲线上斜率最大点决定。对于杜邦990型DTA,R0为0.17℃/mW;对于珀金-埃尔默DSC-2,R0为0.1℃/mW。 A.1.4 非线性校正 非线性校正值根据仪器供应商提供的标准校正手册查找。 A.2 峰温校正示例使用杜邦990型TDA仪对峰温进行校正的典型示例如下:a) 实验条件 升温速率:5℃/min;灵敏度S:0.185mW/cm;热阻R0:0.17℃/mW;峰高H:8.9 cm;峰值:247.2℃(见图A.2)。 b) 三个校正值 升温速率的校正值从表A.1得到:0.15℃; 热延迟校正值按公式(A.1)计算:TLe=8.9×0.17X0.185=0.28(℃); 非线性校正值:根据标准校正手册查为一3.67℃。 c) 校正后的峰温计算 校正后的峰温=峰值+升温速率校正值+热延迟校正值+非线性校正值 =247.2+0.15+0.28+(-3.67) =244.0(℃) 
附录B (资料性附录) 活化能计算示例B.1 计算活化能步骤B.2 计算结果 B.1 计算活化能步骤B.1.1 升温速率与校正过的峰温倒数的对照表见表B.1。表B.1 升温速率与峰温倒数的对照表 
B.1.2 把lgβ与1/T作图,得到的斜率是-3398,见图B.1。 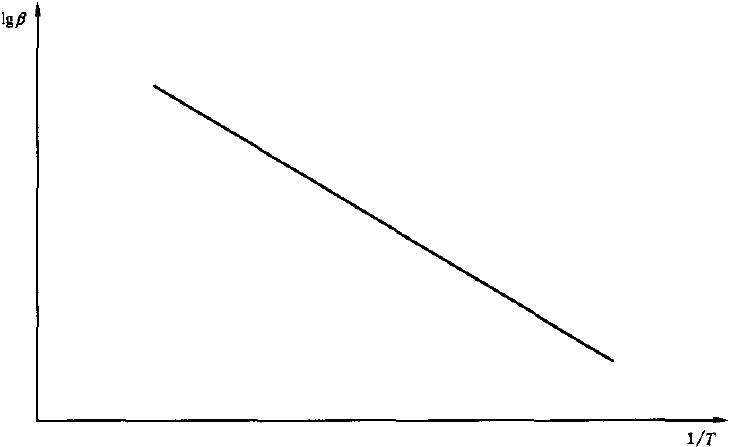
图B.1 计算斜率的示意图 B.1.3 按照公式(1)计算活化能E。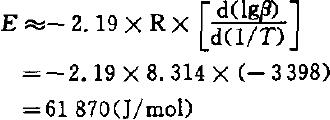
B.1.4 按下述步骤计算精确活化能数值: a) 计算E/RT,其中,T是靠近升温速率中间值的峰温; E/RT=(61870/8.314)(0.002 214 1)=16.48 b) 从表B.2中查找对应E/RT的D值是1.121 5; c) 按照公式(2)计算活化能E值; 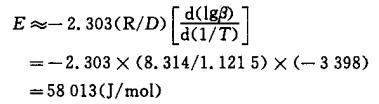
d) 重复a)~c)步骤,计算出精确的E值。 
B.2 计算结果
附录C (资料性附录) 活化能计算的替换方法C.1 计算活化能步骤C.2 计算阿仑尼乌斯指前因子Z的数值 C.1 计算活化能步骤C.1.1 按附录A中所示方法,对峰温进行校正。C.1.2 以一In(β/T²)与1/T计算斜率,其中,β为升温速率,T为校正后的峰温,见表C.1。 表C.1 一In(β/T²)与1/T的关系 
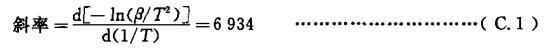
C.1.3 按照公式(C.1)、公式(c.2)计算活化能数值: 
C.2 计算阿仑尼乌斯指前因子Z的数值按照公式(3)计算阿仑尼乌斯指前因子Z数值: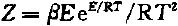
附录D (资料性附录) 恒温试样计算示例D.1 计算速率常数k步骤D.2 计算半衰期 t1/2 D.1 计算速率常数k步骤D.1.1 需要被检验的阿仑尼乌斯动力学数值为:a) 活化能:E=58000 J/mol; b) 指前因子:Z=1.290x106 min-1 D.1.2 在350℃~380℃范围内,按照公式(4)计算速率常数K,计算结果见表D.1。 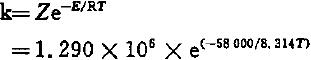
D.2 计算半衰期t1/2根据不同的K值,按照公式(5)计算反应半衰期t1/2,计算结果见表D.1。表D.1 半衰期的计算 
|
1. 本站所有资源来源于用户上传和网络,仅作为演示数据,如有侵权请邮件联系站长!
2. 盗版,破解有损他人权益和违法作为,请各位站长支持正版!
2. 盗版,破解有损他人权益和违法作为,请各位站长支持正版!

 国家标准(推荐)
国家标准(推荐)